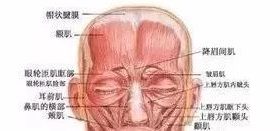
一、肉毒素的作用机理
肉毒素通过抑制神经介质释放,引起肌肉麻痹,因此被广泛应用于医疗和医美产业。在医疗领域中可治疗眼睑痉挛、上下肢痉挛等病症;在医美领域中可除皱、瘦脸等, 还可以其他医美项目结合使用进行联合治疗。
肉毒杆菌毒素(Botulinum Toxin)又称肉毒素,是由肉毒杆菌于厌氧条件下生长时所产生的一类 嗜神经性外毒素。肉毒素共有A、B、Cα、Cβ、D、E、F、G八种类型,其中A型、B型、E型、F型 对人类有毒性,而A型肉毒素毒性最强、应用最广。据资料显示,它是迄今为止科学家发现的毒性最强的一种生物毒素,其毒性相当于等量氰化钾的1万倍。
肉毒素能够有效抑制胆碱能神经介质——乙酰胆碱的释放,从而阻断胆碱能神经传导的生理功能, 引起全身随意肌松弛麻痹。正常情况下,神经末梢会分泌能使肌肉收缩和促进腺体分泌的乙酰胆碱,但肉毒素能与神经末梢结合,抑制神经末梢分泌乙酰胆碱;乙酰胆碱无法分泌,肌肉就无法收缩,腺体就无法分泌,若呼吸肌被麻痹则会致死。因此肉毒素最初被用于生化武器,但因为低剂量局部使用肉毒素可消除肌肉痉挛、除去皱纹,后来也被广泛应用于医疗和美容行业。
(一)肉毒素制剂工艺及评价指标
肉毒素的制备工艺流程大体上分为肉毒杆菌的发酵、分离、提纯、制剂、成品五个阶段。 肉毒素的主要评价指标:
1.赋形剂:药物制剂中除了主药以外的附加物都称为赋形剂或辅料,肉毒素的赋形剂分为医用明胶、人血清白蛋白和不含辅助蛋白。医用明胶来源于猪或牛,提取工艺简单,产量较高,但容易产生排 异反应;人血清白蛋白提取工艺复杂,但安全性高;
2.弥散半径:弥散面积越小,效果越精准,不会影响到注射区域周围的肌肉组织,造成面部表情僵硬 的概率小,更安全。
3.药物稳定性:在生产工艺上,进口肉毒素一般采用真空干燥法,不容易产生抗体,稳定性更强;肉毒素的一般维持时间为4-6个月,其注射效果与医师注射手法及剂量有很大关系。
(二)肉毒素的医美应用
1.抚平动态皱纹
肉毒素仅适用于动态皱纹的抚平,并不适用于静态皱纹。动态皱纹是指作出不同面部表情时出现的皱纹,主要包括眉间纹、抬头纹、鱼尾纹、鼻背纹和眼下细纹,因神经细胞负责传导信号使肌肉收缩从而形成了皱纹。通过注射肉毒素,神经细胞传递的信号将被阻截,有助于放松肌肉并抚平动态皱纹。肉毒素也可与玻尿酸结合使用,以达到更理想的除皱效果。
2.塑形
肉毒素注射瘦脸适用于咬肌肥厚型的脸宽脸大,将肉毒素注射到两侧咬肌,阻断神经与肌肉之间的介质传递,引起肌肉松弛性麻痹萎缩,以达到咬肌体积缩小的作用。瘦脸针从注射到咬肌缩小需要一定的时间,注射一周后咬肌变软,逐步达到松弛状态,一至两个月瘦脸效果最佳,四个月肌肉活动开始恢复,六个月左右效果消失。
3.改善斜方肌、露龈笑
肉毒素可调整肩部和唇部肌肉,从而改善斜方肌、露龈笑等问题。通过在颈部和肩部交界区域内的肌肉中注射肉毒素,可以放松斜方肌和肩胛提肌,有助于提升仪态。通过在鼻唇沟上部注射肉毒素,阻断提上唇鼻翼肌的外侧纤维,抑制上唇肌肉过度运动,使上唇肌肉部分退化,可达到矫正露龈笑的作用。
二、肉毒素市场分析
全球肉毒素行业的应用领域仍以医疗为主。根据华经产业研究院和首尔经济日报统计,2020年全球肉毒素市场规模达到50.9亿美元,2017-2019年全球肉毒素的医疗用途市场规模占比维持在57%左右,2020年达到58.9%,考虑到肉毒素在疾病治疗方面的刚性需求以及其治疗领域适应症的不断扩展,医疗用途在未来较长时间内仍会占据重要地位,同时医美端应用也在快速增长。
1.欧美企业处于领跑
2017年美国艾尔建旗下的Botox产品拥有72%的全球市场份额,独占鳌头;其他的主要竞争者包括Ipsen旗下的Dysport(15%)、MERZ旗下的Xeomin(4%)和Medytox旗下的Medytoxin(3%)。总体来看欧美厂商瓜分了大部分的全球市场,亚洲厂商在国际上尚未取得明显优势。
2.韩国肉毒素市场本土品牌竞争激烈。
2018年Hugel旗下的Botulax占据了最大的市场份额(40%),其他本土竞争者包括Medytox旗下的 Medytoxin(35%)、大熊制药旗下的Nabota(7%);海外进口产品则包括Botox、Dysport和 Xeomin,占比相对较小。2020年Medytox受罚后市场格局发生改变,Medytox被迫退出肉毒素市场。
3.中国正规肉毒素市场规模逐年增长并进一步扩张
艾媒咨询数据显示,2019年中国正规渠道肉毒素市场规模为48.6亿元,同比增长24%;中国肉毒素占非手术类医美项目的32.7%,远低于美国的76.1%,且肉毒素注射是中国轻医美用户最偏好的top5项目之一,发展潜力大。我国肉毒素依据毒麻药品审批,较普通的医疗器械类产品审批流程更长,从立项到获批需八年或更长。毒麻类药品准入门槛更高、研发难度较大、耗时更久,审批的总流程至少需要8年以上才能走完。肉毒素行业的门槛因此极高,不仅需要突破技术上的难关,还需经历层层审核,确认合格方能上市。
目前国内上市公司大多以代理及股权投资的方式布局肉毒素行业,国药控股为保妥适在国内的总经销商,四环医药取得乐提葆的独家代理权,华东医药获得Jetema肉毒素产品的独家代理。另一些企业采取股权投资合作研发的方式进行长期稳定布局,如爱美客与韩国Huons合作开发Hutox,华熙生物与Medytox合作研发Meditoxin等。
中国肉毒素市场集中度较高,2020年以前一直被进口和国产两个品牌垄断:由于肉毒素严格的审 批流程和高进入门槛,我国乃至世界获批的正规肉毒素产品都较少。自2009年保妥适获批进入中国市场,国内正规肉毒素市场保持保妥适和兰州衡力 二分天下,艾尔建作为全球医美领军者,在中国的市场份额也在不断提升,2018年达到53.52%,首次超过衡力。
现有市场中保妥适占据销售额优势,国产衡力凭借性价比优势占据销量领先:进口品牌保妥适采用人血清白蛋白为赋形剂,采用真空干燥工艺,且弥散度小,临床时间长达20年,在安全性与稳定性等方面优于国产衡力,售价较高,定位高端,2019年保妥适以26%的销量占据了56%的销售额。衡力凭借高性价比销量占比74.3%,销售额占比44.4%,两个品牌几乎分掉全部市场份额。2020年随着新批文落地,正规肉毒素市场参与者增加:2020年以前我国正规肉毒素市场保持。
2020年吉适与乐提葆正式获批,我国正规肉毒素市场参与者增加,市场将格局转变。
肉毒素市场相比于玻尿酸进入壁垒更高,国内企业多以代理或合作进行布局。肉毒素目前正规产品较少,发展潜力较大,属于医美行业的蓝海领域,吸引大量企业积极布局市场。中国企业主要以代理与股权投资的方式切入肉毒素市场,目前已有爱美客、昊海生科、华东医药、复星医药等在内的多家厂商,与韩国、美国、德国肉毒素生产商签署合作协议,预计未来几年,正规肉毒素市场将再添猛将。
未获CFDA批准的水货产品对比
三、相关企业研究分析
1.艾尔建
成立于1950年,是一家跨国健康医疗公司,前身为眼科药品生产商,后通过收购肉毒素产品Oculium等逐步发展成为医美巨头,其产品覆盖面部美学、身体塑形、整形、皮肤护理等领域。2020年5月艾伯维以640.84亿美元收购艾尔建,并将其打造成一个专营医美产品的全球业务公司——艾尔建美学。
保妥适于1989年首次被FDA批准上市,用于治疗眼睑痉挛和斜视,是首个获批的A型肉毒素产品,之后进行不断创新,在治疗与医美领域获批的适用症达26项,包括慢性头痛、膀胱过度活动症、腋窝多汗症等,是全球获批适应症最多的神经毒素类药物。目前,保妥适在100 多个国家或地区获得上市批准,全球产量超过1亿瓶。
2019年艾尔建医美业务全球收入达42.53亿美元,其中保妥适收入达16.63亿美元,2015-2019年CAGR为17.9%,2021年Q1保妥适全球净收入4.77亿美元,同比增长44.7%,2018年保妥适全球市占率仍高达65%,占据绝对市场地位。
业务分拆,医美业务单独剥离:2020年艾伯维收购艾尔建,并将其业务进行分拆,眼科护理与特药业务(保妥适医学产品、中枢神经、妇女健康和消化产品)将被整合进艾伯维现有的业务结构,医美业务包括保妥适、乔雅登及酷塑等被单独剥离,并创建艾尔建美学全球业务公司对其进行专项运营。
2020年2月艾尔建宣布旗下全新尖端工厂Biologics2(B2)正式启用,新工厂位于爱尔兰梅奥郡韦斯特波特镇,总投资额达1.6亿欧元,B2工厂拥有全新厂房与生产设备,用以满足全球对艾尔建产品日益增长的需求,另外,配备先进微生物及细胞实验室,支持公司下一代生物制剂的研发与创新。新厂投产,揭开艾尔建肉毒素产品及其他生物制剂研发与增长的新篇章。
2.兰州生物(衡力)
国内唯一肉毒毒素生产商:兰州生物技术有限公司始建于1934年,隶属中国医药集团有限公司旗下的中国生物技术有限公司,1993年公司自主研发的衡力肉毒素上市后,中国成为继美国和英国后第三个能自行生产肉毒素产品的国家。
公司主要从事预防类制品、治疗类制品、诊断试剂等生物制品的生产、研发与经营,主要产品包括口服轮状病毒活疫苗、A群C群脑膜炎球菌多糖疫苗、B型流感嗜血杆菌结合疫苗以及注射用A型肉毒毒素。
迄今衡力累计使用人次逾2700万,在中国,每注射10支A型肉毒素就有8支是衡力,凭借其超高的性价比在2018年以前其销售额超过保妥适。衡力使用Hall菌株,分子量均一,单体纯度在99.5%以上,采用离子交换层析法纯化率较高,不良事件发生率20.22%,低于国际同类产品24%的水平。当前,衡力远销韩国、巴西、俄罗斯等34个国家与地区。
3.四环医药
公司成立之初,专注于心脑血管疾病领域的药物研 图42:近五年业绩有下滑趋势发与销售,先后收购北京四环、深圳四环、山东轩竹等,完善心脑血管产品线。受国家药品重点监控目录等政策的影响,公司近五年业绩有下降趋势。
公司2014年开始进军医美行业,与韩国Hugel签署独家代理其A型肉毒素产品及玻尿酸产品的合作协议,2017年又与奥地利Croma合作,推出主打中高端市场的Princess系列玻尿酸产品等,预计给公司带来业绩增量
四环医药于2014年与韩国Hugel合作,独家代理其A型肉毒素产品“乐提葆”,布局医美赛道,2020年10月“乐提葆”获NMPA认证, 成为国内第四款获批的A型肉毒素产品,正式成为正规军的一员。
“乐提葆”定位轻奢肉毒,是一款进口入门级的肉毒素,价格上定位在衡力与保妥适、吉适之间(保妥适>吉适>乐提葆>衡力),并采用独有的CBFC26菌株,品质更高,弥散度低,维持时间更长。
4.爱美客
爱美客成立于2004年,是国内知名医美针剂制造商,其产品覆盖玻尿酸、肉毒素、童颜针,打造了全品类的医美针剂产品矩阵,特别在玻尿酸针剂市场的五个“首款”奠定了行业领先地位。
2018年9月与Huons签订合作研发A型肉毒素及独家经销的协议,相关产品目前已进入临床三期阶段,获批上市可期。其他在研项目布局蓝海市场,如“童颜针”产品已获批,有望为企业带来新的利润增长点。
拟斥资8.86亿元收购韩国肉毒素公司:2021年6月公司宣布拟用8.86亿元收购Huons Bio部分股权。Huons Bio是韩国老牌医药集团Huons Global分拆出 的肉毒素业务子公司。目前该收购计划暂缓。
5.昊海生科
公司自2007年成立就以收并购的方式扩张业务版图,完成以医用透明质酸钠/玻璃酸钠和医用几丁糖为核心的生物医用材料的行业重组,有效扩充了产品品类。截至目前,已形成眼科、整形美容与创面护理、骨科、防粘连及止血四大业务板块,并处于行业领先地位。
2021年3月,昊海生科拟以3100万美元认购Eirion新发行的A轮优先股,持有大约13.96%的股份,根据协议Eirion授权昊海生科外用涂抹型A型肉毒素产品ET-01、经典注射型A型肉毒素AI-09、治疗脱发白发用小分子药物产品ET-02在中国大陆、香港及澳门、台湾地区的独家研发、销售、商业化许可,许可协议的预付款为800万美元。
Eirion是一家位于美国波士顿的生物医药研发公司,主要从事A型肉毒素及小分子药物的研发与生产。此次引进的肉毒素产品中ET-01为创新型的外用涂抹式肉毒素产品,目前国内还没有相似的产品上市,适用于鱼尾纹及腋下多汗症的治疗;AI-09为液体注射型肉毒素,相比传统的冻干粉形式,使用更为便捷。
6.华东医药
华东医药成立于1993年,最初以医药制造为主业,后逐步发展为医药制造,医药商业及医美三大业务板块。2020年营收336.83亿元,归母净利润28.2亿元。
医药工业:专科、慢病用药及特殊用药领域的研发、生产与销售,重点在抗肿瘤、内分泌、自身免疫三大核心治疗领域;2020年营收占比33.84%;医美业务:主营面部微整形与皮肤管理领域产品和器械的研发、生产与销售,依托Sinclair,西班牙High Tech,以及美国R2,瑞士Kylane四个全球化研发中心,及荷兰、法、美、瑞士及保加利亚五个全球化生产基地,构建全球化医美全产业链布局;2020年营收占比0.95%,2020年8月,华东医药与Jetema签署战略合作协议,获得其A型肉毒素产品在中国的独家代理权。
Jetema是韩国的一家主营医美生物制药与医美器械的上市公司,主要产品包括透明质酸钠凝胶、肉毒素、医疗设备等,是世界上唯一一家同时获得A/B/E型肉毒素的公司。
2021年4月Jetema宣布其肉毒素产品The Toxin(用于改善中重度眉间纹)完成了一期临床试验,二期临床于去年6月已获批,目前正在向韩国食品医药品安全厅申请三期临床试验,并同时在中国进行启动注册报批工作,预计2024年可在中国获批上市。
Jetema的肉毒杆菌菌株是2017年从英国引进的,来源相对安全,2020年4月Jetema与韩国历史最久的Dongwha Pharm制药公司签署合作协议,共同开发肉毒素在医美以外的新适应症,Jetema肉毒素适用症的扩展,将使华东医药在肉毒素市场占据更有利地位
7.复星医药
复星医药成立于1994年,业务范围涵盖制药、医疗器械与医学诊断、医疗服务、医药商业,是国内领先的国际化医药健康产业集团。营收稳步增长,毛利率近年来保持50以上,业绩稳定。
独家代理RTOO2:2018年12月,复星医药控股子公司复星医药产业与Revance签订许可协议,Revance授权复星医药产业在区域内及领域内独家使用、进口、销售及其他商业化(不包括制造)含有Daxibotulinumtoxin A型肉毒杆菌毒素的注射用药物RT002,复星医药根据协议向Revance支付至多8800万美元的许可费以及支付相应的销售里程碑款项。Revance成立于1999年,2014年于纳斯 达克上市,专注于新型肉毒素产品在美容及治疗适应症的研发、生产与商业化。
RT002是一种有效成分为Daxibotulinumtoxin A型肉毒素的长效神经调节物,其最大的特性是长效持久,原因在于采用专利胜肽技术TransMTS将150kDA的A型肉毒素与稳定赋形剂胜肽进行结合,在不含动物性成分与人体白蛋白的基础上,可增强产品的稳固性进而延长作用时间。可用于缓解中到重度眉间纹以及治疗颈部肌张力障碍、痉挛等疾病。
2020年12月,RT002用于中到重度眉间纹适应症启动Ⅲ期临床,目前处于美国FDA上市申请阶段。2021年1月启动第二项Ⅲ期临床试验,用于治疗孤立性肌张力障碍。
如有相关兴趣,可以作者联系